Leptospirose : vecteurs et sérogroupes
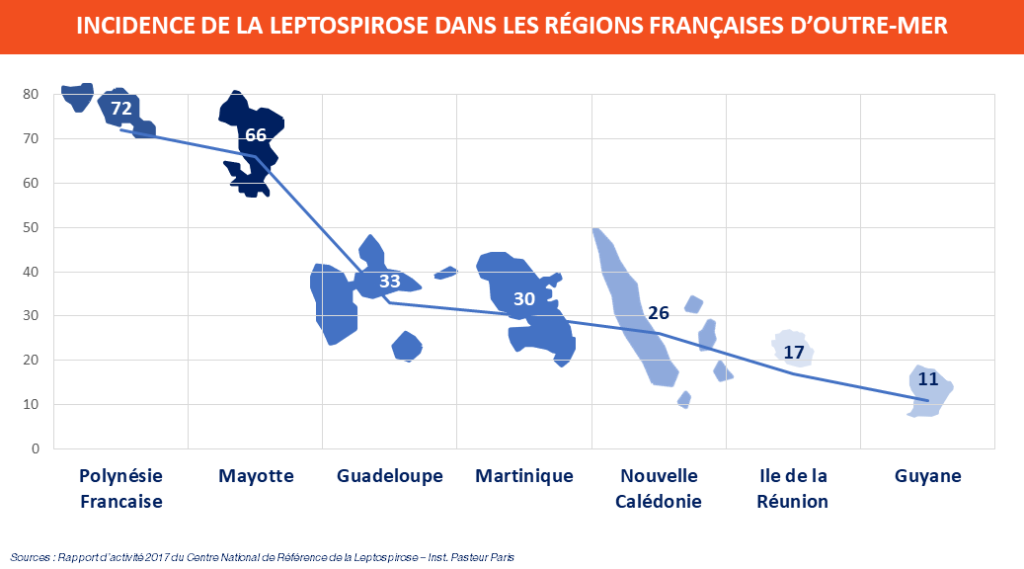
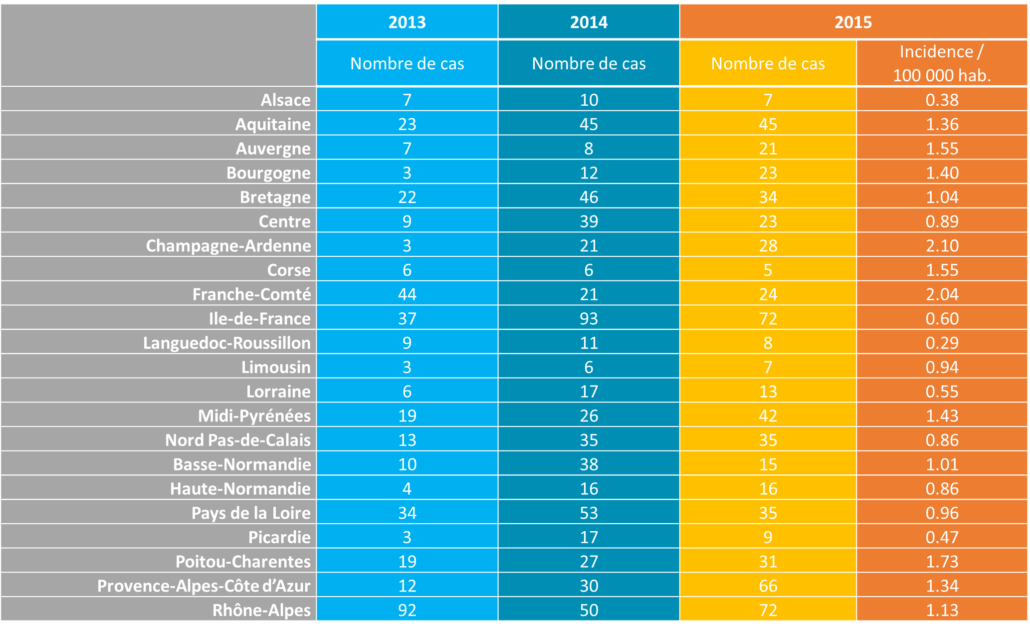
En France métropolitaine, en 2013, le Centre National de Recherche des Leptospires de l’Institut Pasteur de Paris a recensé l’incidence des cas de leptospirose la plus élevée de ces dix dernières années (1). Mais quelle leptospirose ? En effet on pourrait parler de leptospiroses tant il y a de diversité dans le genre Leptospira.
Les leptospires font partie du phylum des spirochètes, microorganismes qui possèdent des caractéristiques uniques dans le monde bactérien : spiralés et dotés d’un organe locomoteur interne, l’endoflagelle, ils sont très mobiles même dans les milieux les plus visqueux. Ce sont des bactéries très répandues dont les genres pathogènes sont à l’origine de maladies humaines telles que la maladie de Lyme, la syphilis, ou encore la leptospirose.
On divise généralement le genre Leptospira en deux groupes : Leptospira biflexa, souches saprophytes et aquicoles, et Leptospira interrogans, souches pathogènes. A ce jour la littérature a décrit 21 espèces de leptospires et plus de 300 sérovars regroupés en une vingtaine de sérogroupes, une classification toujours en évolution(1).
21 espèces de leptospires et plus de 300 sérovars regroupés en une vingtaine de sérogroupes
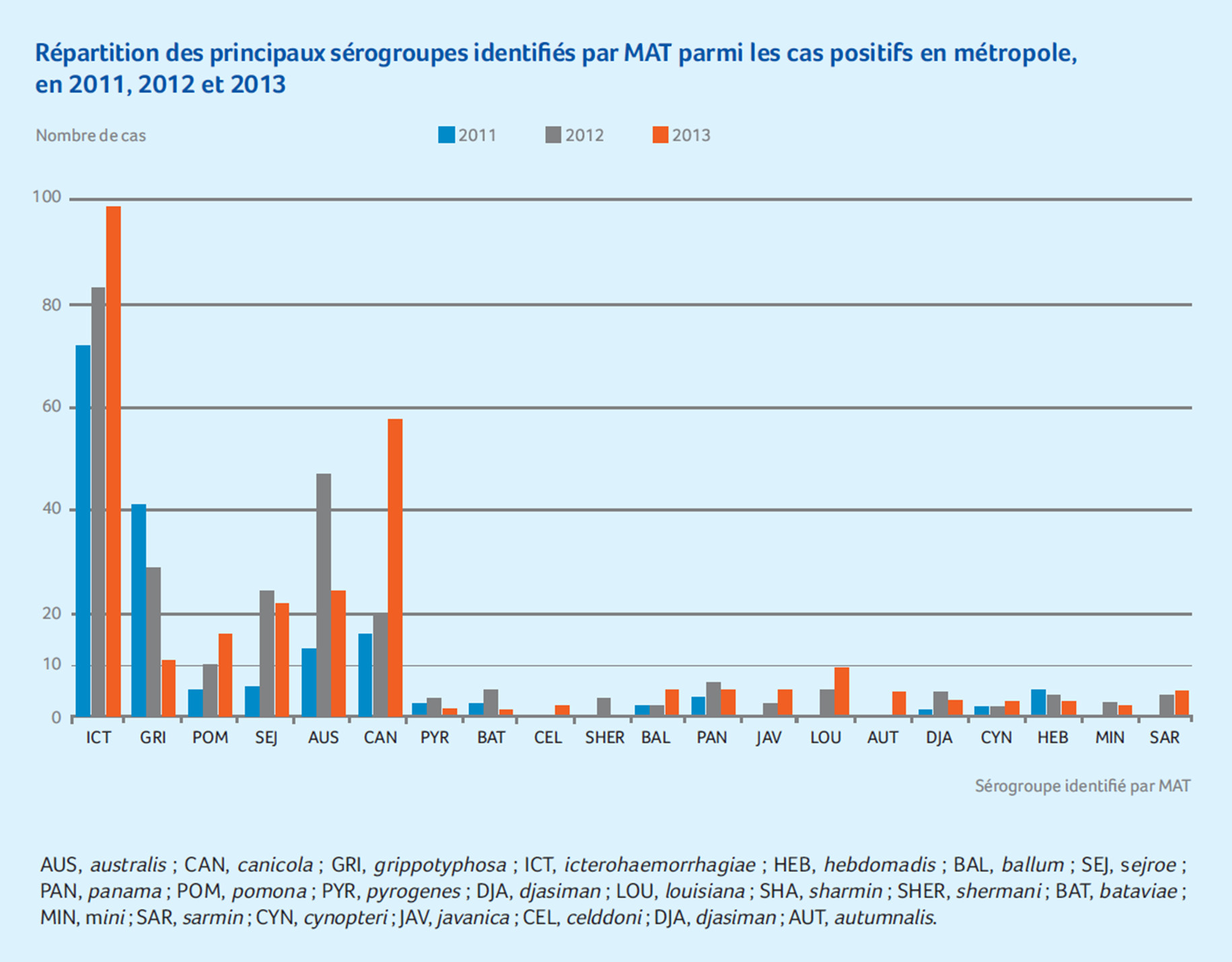
Si on peut recenser un très grand nombre de sous-ensembles, il semble cependant que certains sérogroupes du genre Leptospira interrogans soient davantage présents chez certaines espèces porteuses. Ainsi, par exemple, en France le sérogroupe australis semble se retrouver majoritairement chez les bovidés, le sérogroupe canicola chez les canidés, tandis que les rongeurs, les ovins et les porcins sont, entre autres, les porteurs privilégiés du sérogroupe icterohaemorrhagiae(2). Et si les mammifères sont le plus souvent cités, certaines études ont mis en évidence la présence d’anticorps contre les leptospires chez certains reptiles (serpents, lézards, tortues)(3).
Certaines espèces sont dites porteuses saines, répandant les bactéries dans l’environnement via leurs urines mais ne manifestant aucun signe clinique de l’infection, comme les rats par exemple ; d’autres peuvent présenter des signes cliniques mais ceux-ci sont très variés, comme c’est notamment le cas pour les animaux d’élevage et l’Homme, hôte accidentel de la bactérie. Ainsi le cheval peut développer des affections localisées, subaïgues ou chroniques comme les uvéites récidivantes(4), la leptospirose peut également être à l’origine d’avortements ou d’arrêts brutaux de la production de lait chez les bovins(5), etc.
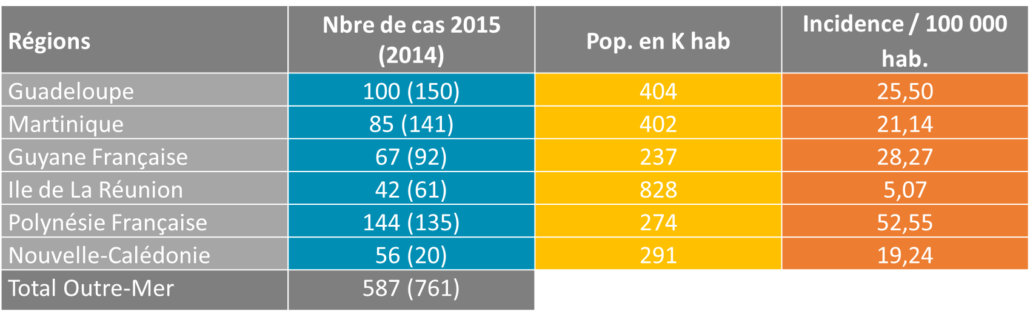
L’épidémiologie humaine de la maladie est en grande partie fonction du réservoir, c’est-à-dire de la faune locale, déterminant les souches circulantes au sein d’une région. Mais pas seulement. Certaines régions présentent des particularités comme Mayotte où le sérogroupe le plus représenté est le sérogroupe mini tandis qu’il est très peu représenté sur les autres îles environnantes et dans le reste du monde(6).
Cependant la répartition des sérogroupes dans les cas d’infections humaines reste très mal connue dans de nombreux pays du fait de la difficulté à poser un diagnostic et des moyens nécessaires à l’identification de la souche en cause. En effet les centres de référence qui pratiquent le test MAT et surveillent les données épidémiologiques locales restent très peu nombreux de par le monde(1).