Geneviève André-Fontaine,
professeur d’infectiologie
retraitée de l’Ecole Nationale
Vétérinaire de Nantes
Les leptospires : une résistance étonnante, même à 4°C
Encore très récemment, nous pensions qu’une température de 15 à 30°C était indispensable à la survie des leptospires dans le milieu naturel. Or, une étude publiée par Geneviève André-Fontaine, professeur d’infectiologie retraitée de l’Ecole Nationale Vétérinaire de Nantes(1), montre que les leptospires du sérogroupe Icterohaemorrhagiae peuvent survivre jusqu’à 300 jours maximum dans une eau douce à seulement 4°C. Une résistance exceptionnelle et inattendue, qui pourrait impacter l’estimation du risque de contracter la leptospirose sur le territoire français…
« Dans les eaux de
surface, les leptospires
sont capables de résister
pendant des temps
très longs. »

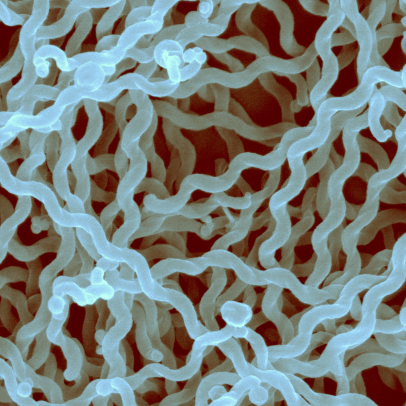
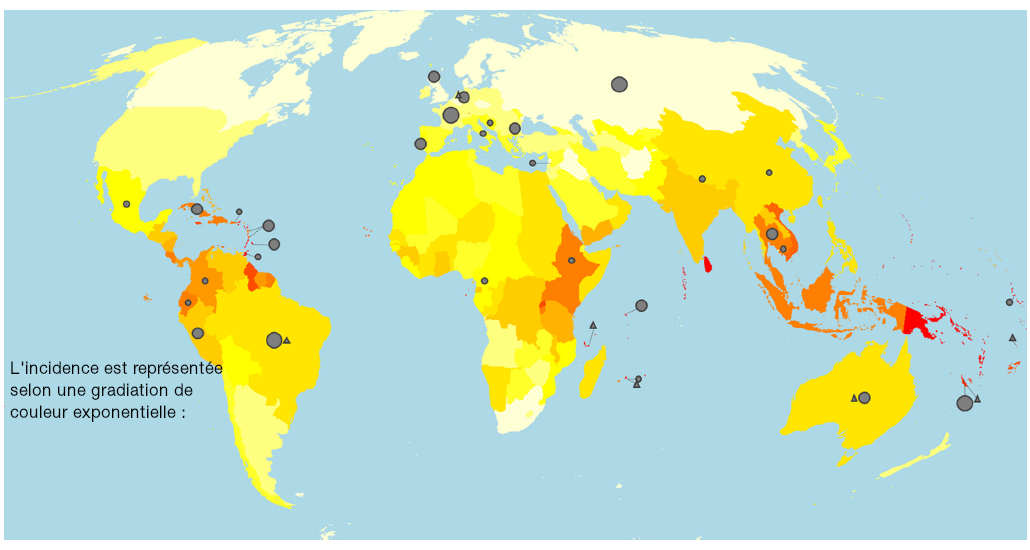
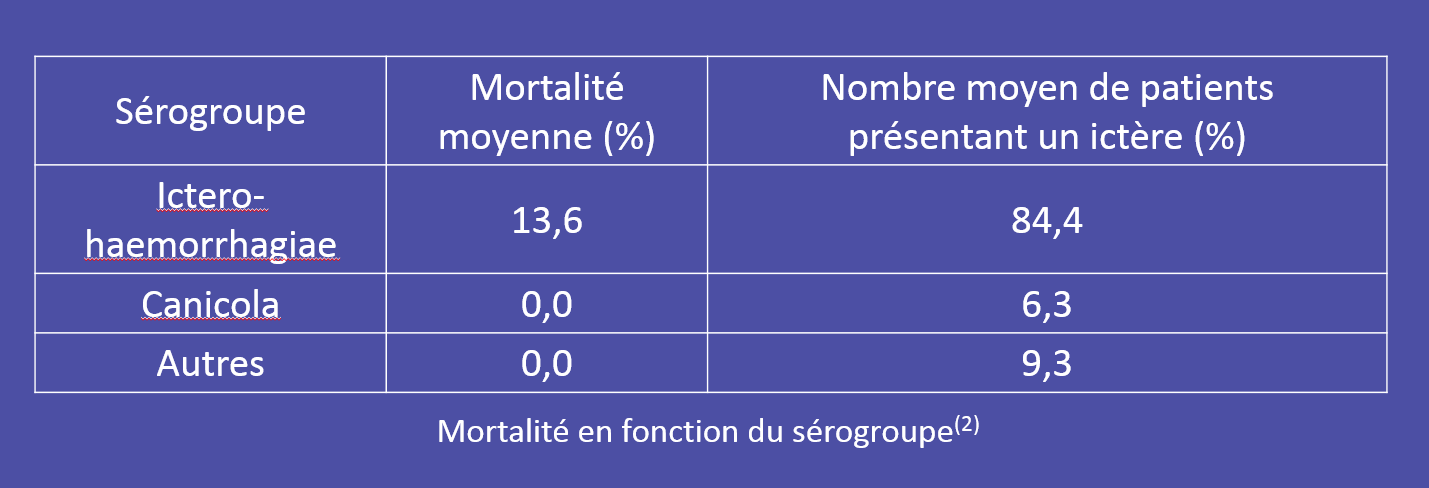
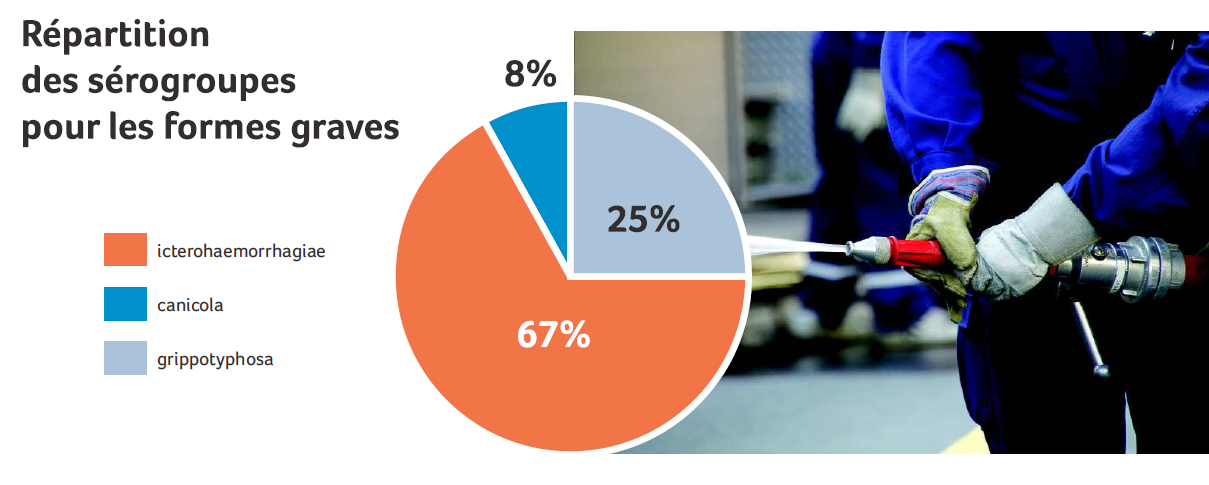
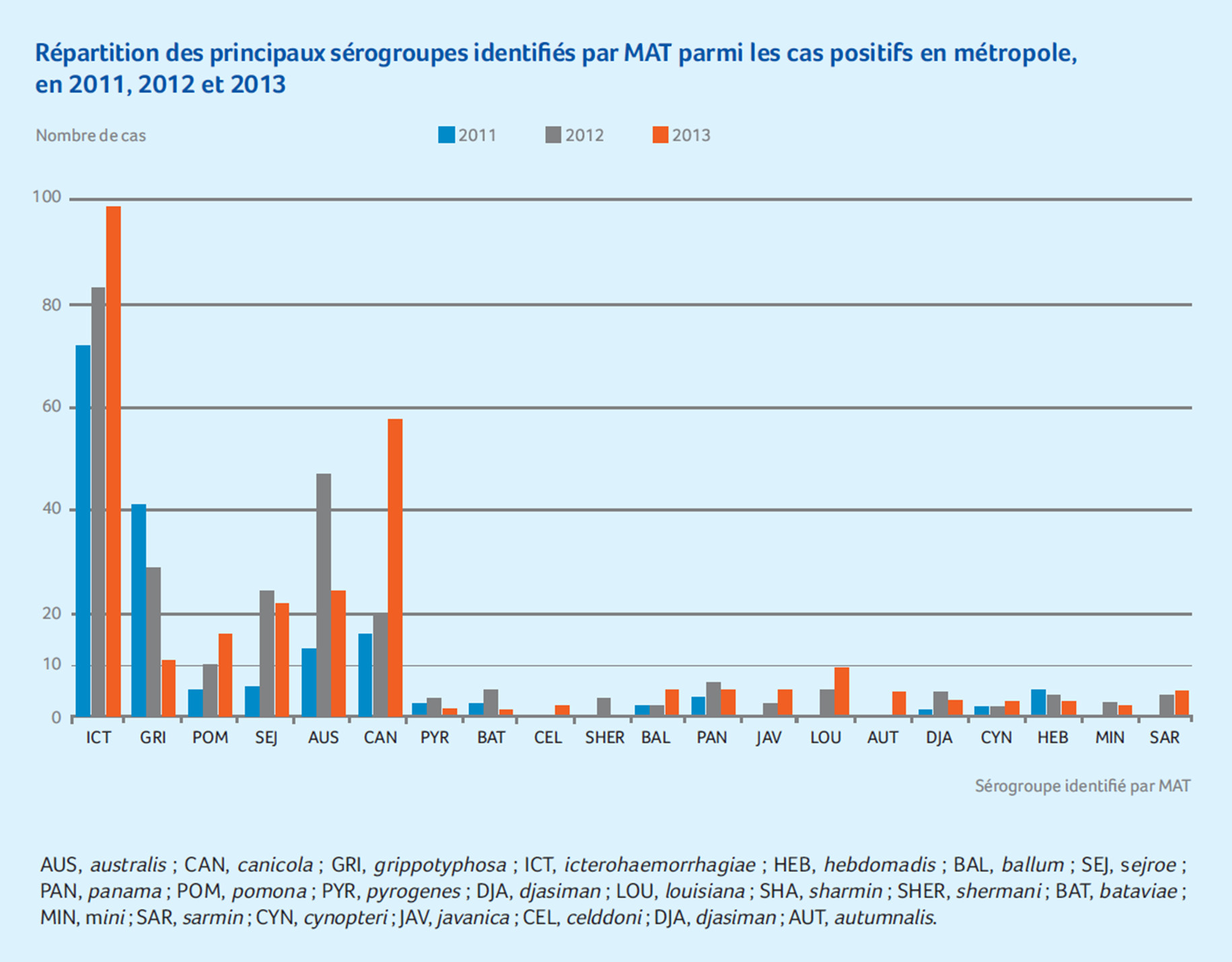
Bactéries responsables de la leptospirose, les leptospires sont des filaments spiralés extrêmement fins, dotés d’une mobilité extraordinaire dans les milieux liquides. Les leptospires du sérogroupe Icterohaemorrhagiae sont les plus fréquemment rencontrés en clinique humaine en France, et responsables des formes les plus graves.(2)
La transmission de la maladie peut s’effectuer soit par contact direct avec les urines d’animaux infectés, principalement de rongeurs, soit par contact avec les eaux douces souillées par ces urines.
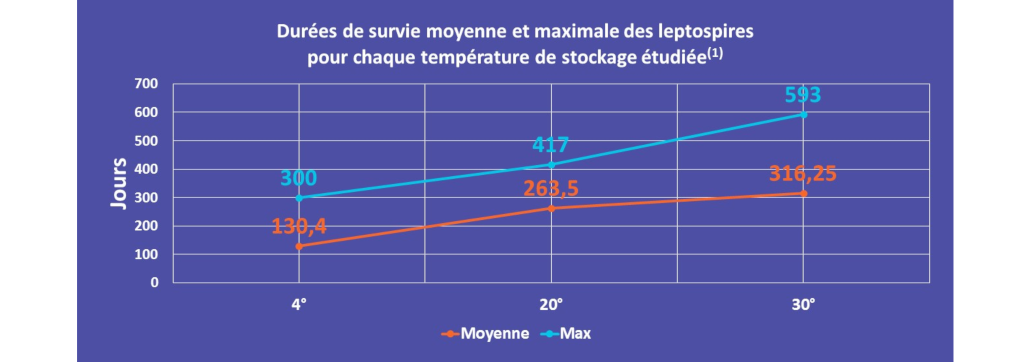
Mais combien de temps les leptospires peuvent-ils résister dans ces eaux douces, sans nutriment, à des températures qui peuvent être très variables ? C’est à cette question que répond le professeur Geneviève André-Fontaine dans une étude publiée en 2015 intitulée « Waterborne Leptospirosis: Survival and Preservation of the Virulence of Pathogenic Leptospira spp. in Fresh Water » (1). L’équipe de recherche a inoculé une souche pathogène du groupe Icterohaemorrhagiae dans différentes eaux naturelles et pures, commercialisées pour la consommation et ne contenant donc aucune matière organique permettant aux bactéries de survivre. Des échantillons de ces eaux contaminées au laboratoire ont ensuite été conservés pendant 20 mois à une température de 4°C, 20°C ou 30°C. Les analyses effectuées ont démontré que la survie moyenne des leptospires était de 130 jours à 4°C, 263 jours à 20°C et 316 jours à 30°C.
L’étude met en évidence la capacité des leptospires à survivre dans des eaux douces pendant des périodes extrêmement longues, mais également à préserver leur virulence.

Un impact sur l’évaluation du risque en France métropolitaine ?
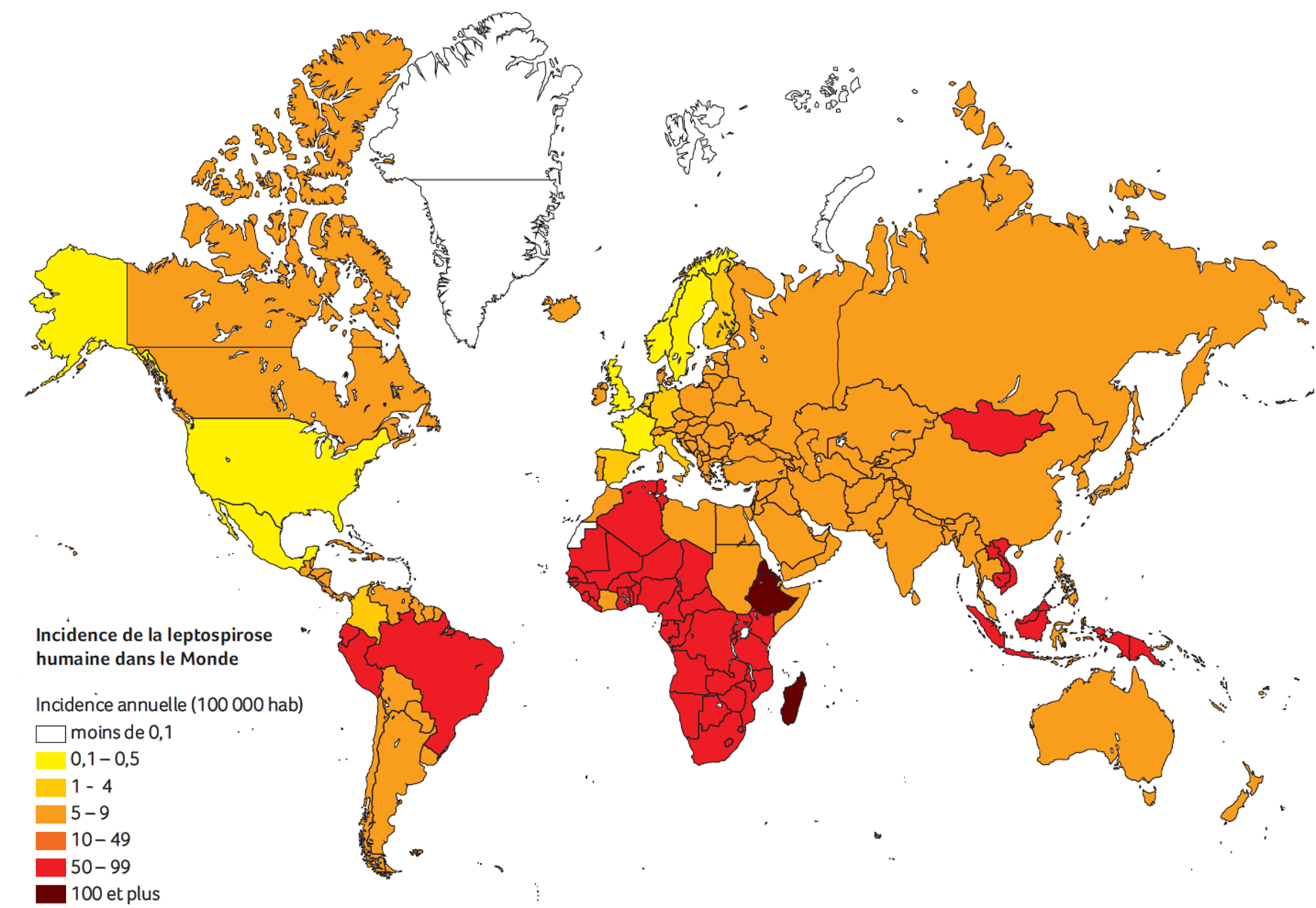
Ces résultats apportent un nouvel éclairage sur le risque d’exposition à la leptospirose en zone non tropicale. En effet, sur la base des éléments mis en avant par Ian R. Ferguson en 1994(3), la communauté scientifique et médicale estimait que la bactérie pouvait survivre jusqu’à 6 mois dans des substrats humides, selon les conditions. L’eau froide des rivières, en particulier, était jugée peu favorable aux leptospires.
Or, on sait désormais que même si elles ne s’y multiplient pas, les bactéries du sérogroupe Icterohaemorrhagiae sont capables de résister plus de dix mois dans l’eau à une température de 4°C, et au moins 20 mois à 30°C, en conservant leur caractère pathogène. L’estimation du risque lié à la pratique d’activités professionnelles mais aussi de loisirs dans les rivières et plans d’eau français, même en montagne, pourrait donc prendre une nouvelle dimension, alors que ces activités de loisirs sont en plein développement.
L’exposition au risque est à pondérer en fonction des conditions climatiques, et également en fonction du nombre et de la nature des animaux réservoirs de ces bactéries présents dans l’environnement. Ces animaux porteurs apparemment sains peuvent en permanence contaminer et re-contaminer l’eau par leurs urines.
A la suite des récentes inondations qui ont touché le Nord de la France, une recrudescence de rats a pu être observée dans les zones sinistrées(4).A la lumière de ces nouvelles connaissances, on peut se demander si, en favorisant à la fois la dissémination et la survie des leptospires, la montée des eaux de la Seine et de ses affluents pourrait conduire à une hausse du nombre de cas de leptospirose dans les régions touchées…
« Rappel :
les microlésions cutanées
constituent la principale
porte d’entrée des
leptospires dans
l’organisme. »
Loisirs aquatiques : « Mieux vaut être conscient du risque et s’en prémunir ». Le témoignage de Nicolas, 37 ans*
« La leptospirose est considérée comme une maladie des égoutiers et l’on ne s’attend pas à y être exposé dans un tel contexte…»
En avril 2015, Nicolas participe à une course à obstacles en Sologne. Le principe : courir, franchir des obstacles, ramper dans la boue, nager dans des étangs…, sur une distance totale de 10 kilomètres. Sur ce parcours, Nicolas s’écorche les genoux en rampant dans une buse d’eau pour passer sous un petit pont.
Une semaine plus tard, alors qu’il part en déplacement professionnel en Afrique, lors de son vol aller, il est pris de violents frissons, transpire beaucoup, ressent des courbatures dans tout le corps et de fortes douleurs lombaires. Malgré le paracétamol, son état ne s’améliore pas et quand il rentre en France, au bout d’une semaine, un ictère visible au niveau des yeux, une desquamation importante et des douleurs aux genoux s’ajoutent à la liste de ses symptômes. Il est alors pris en charge par les urgences puis placé en isolement, son récent séjour en Afrique faisant craindre un cas d’Ebola. Après perte de connaissance, son état semble de plus en plus critique et le pronostic vital engagé, il pense que c’est la fin.
Les tests biologiques permettent alors de poser un diagnostic de leptospirose. C’est à ce moment-là que le lien est fait avec la lésion aux genoux… Grâce au traitement antibiotique, Nicolas est tiré d’affaire. « J’ai probablement été sauvé par le fait d’avoir bu beaucoup d’eau pour obliger mes reins à fonctionner », confie-t-il. Aujourd’hui, il regrette que les participants à ce type d’activités ne soient pas plus informés sur le risque de leptospirose et les moyens de prévention adéquats !
Références bibliographiques
1. Andre-Fontaine G, et al. Waterborne Leptospirosis: Survival and Preservation of the Virulence of Pathogenic Leptospira spp. in Fresh Water. Curr Microbiol. 2015 Jul;71(1):136-42.
2. Rapport annuel d’activité 2015 pour l’année d’exercice 2014 du Centre National de Référence de la Leptospirose, Institut Pasteur Paris
3. Ferguson IR. A European Perspective on Leptospirosis. Microbiology Europe 1994; Jan-Feb: 8-11
4. http://www.larepublique77.fr/2016/06/14/inondations- une-campagne-pour-eviter-la-multiplicationdes- rats-2/
* Propos recueillis par Nathaly Mermet, journaliste scientifique.